W gospodarstwie komercyjnym prowadzonym na dużą skalę (>2000 loch) we wschodnich Chinach zgłoszono nietypowy objaw zmętnienia oczu i ślepoty u kilku miotów prosiąt ssących. Lochy normalnie produkowały mleko i nie stwierdzono zaburzeń w przyjmmowaniu pokarmu. Liczba martwo urodzonych i słabych świń była nieco wyższa od normalnego poziomu, a śmiertelność przedodsadzeniowa była podwyższona. Ślepotę, zmętnienie rogówki i obrzęk okolicy oczu obserwowano u kilku świń w każdym z kilku miotów. (Rysunek 1).
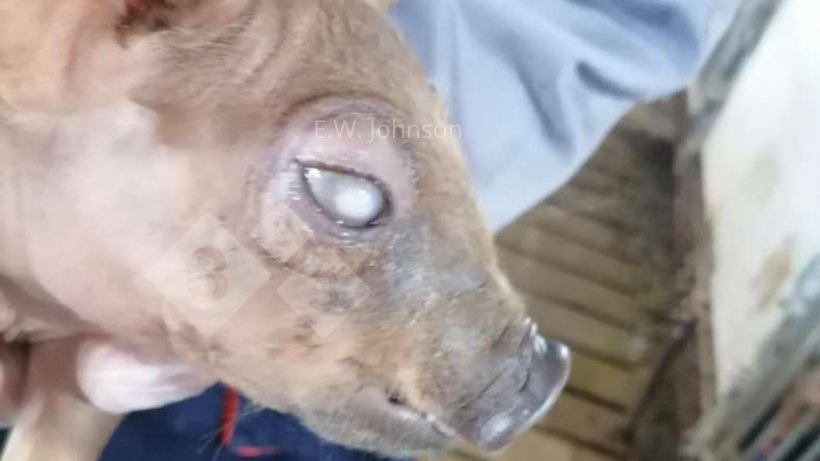
Ryc. 1. Świnia ze zmętnieniem rogówki.

Dotknięte chorobą świnie były apatyczne, ospałe i niezdolne do ssania. Stwierdzono nieco wyższą częstotliwość poronień, ale nie obserwowano wyraźnych przypadków ronień masowych. Liczba zmumifikowanych świń mieściła się w granicach normalnych parametrów. Nie odnotowano żadnych innych objawów klinicznych. Szybkie sprawdzenie dokumentacji hodowlanej wykluczyło możliwą przyczynę genetyczną, ponieważ chorobę stwierdzano u niespokrewnionych linii genetycznych.
Diagnostyka różnicowa obejmowała rubulawirusa świń (choroba niebieskich oczu) i bakteryjne zakażenie oka. Choroba niebieskich oczu jest wywoływana przez paramyksowirusa i uważa się, że występuje endemicznie w niektórych częściach Meksyku. Powoduje ona chorobę ośrodkowego układu nerwowego, zapalenie płuc i problemy z rozrodem u świń hodowlanych, w tym zapalenie gruczołu sutkowego i uszkodzenie rogówki u knurów, ale nie stwierdzono jej występowania w Chinach ani nigdzie poza Meksykiem. Wstępne rozpoznanie choroby niebieskich oczu powinno być postawione na podstawie obserwacji nietypowych objawów klinicznych i potwierdzone metodą PCR oraz izolacją wirusa.
Niedobór witaminy A mógłby spowodować poważne zmiany oczne, ale jest to mało prawdopodobne w tym dużym stadzie komercyjnym karmionym nowoczesną dietą.
Diagnostyka
Jedna z zarażonych świń została humanitarnie uśmiercana i zsekcjonowana przez personel gospodarstwa. Do laboratorium przekazano świeże i utrwalone w formalinie tkanki (wątroba, węzły chłonne, mózg) oraz świeże oczy prosięcia ze zdjęcia (ryc. 1).
Personel gospodarstwa nie odnotował żadnych poważnych zmian patologicznych poza zmianą oczną. Płyn śródoczny zaaspirowany z oczu wydawał się przejrzysty i bez zmian. Wymazy płynu z oczu wybarwionego barwnikiem Giemsy wykazały obecność kilku komórek jednojądrowych i kilku bakterii o kształcie pałeczek. Z płynu ocznego izolowane są nieliczne, niepowiększone szczepy Escherichia coli. Prawdopodobieństwo przyczyny bakteryjnej zostało wykluczone. Węzeł chłonny, mózg i wątroba utrwalone w formalinie były poddawane szybkiej obróbce parafinowej w celu uzyskania wycinków tkanek, które zostały barwione metodą H&E.
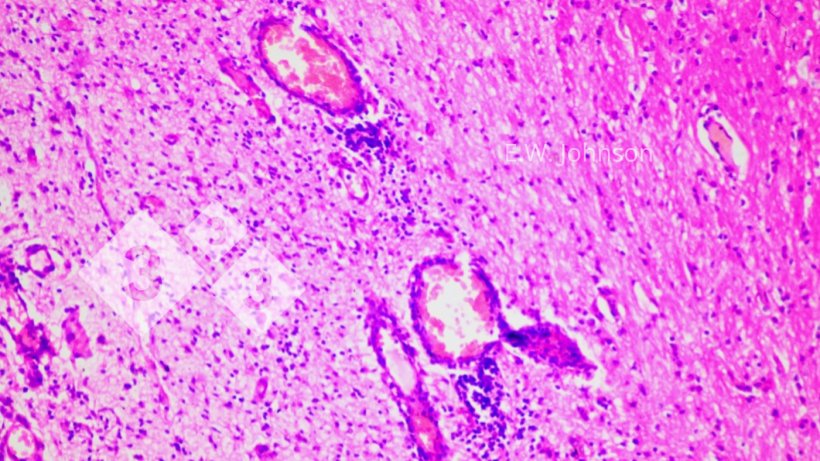
Ryc. 2. Nacieki okołonaczyniowe i glejoza. Mózg.
Badanie mikroskopowe mózgu ujawniło zapalenie opon mózgowo-rdzeniowych z naciekiem okołonaczyniowym i glejozą (ryc. 2) oraz naciek opon mózgowo-rdzeniowych z mieszanymi jednojądrowymi i wielojądrowymi komórkami zapalnymi (ryc. 3). Ryc. 3. Zapalenie opon mózgowych z komórkami jednojądrowymi i kilkoma wielojądrowymi. Mózg.
W wątrobie występowała ogniskowa martwica, a w tkance otaczającej obszary martwicy pojawiają się amfofilne wtręty wewnątrzjądrowe (ryc. 4). Postawiono wstępne rozpoznanie rzekomej wścieklizny (PRV, choroba Aujeszky'ego).
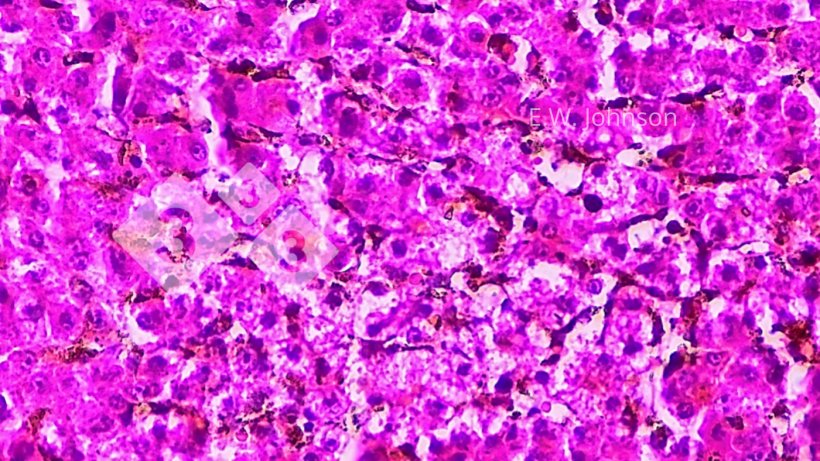
Ryc. 4. Ogniskowa martwica wątroby z okazjonalnymi amfofilnymi wtrętami wewnątrzjądrowymi w strefie okołomartwicowej. Wątroba.
W wyniku PCR w płynie z ciała szklistego oka uzyskano amplifikację DNA alfaherpeswirusa 1 (Pseudorabies) US8 ("unique-short" 8) genu kodującego gE, (glikoproteinę E), co potwierdza obecność wirusa wścieklizny rzekomej typu dzikiego. Sekwencjonowanie amplifikowanego fragmentu US8 ujawnia, że wykryty wirus łączył się z ostatnio pojawiającymi się szczepami wariantowymi PRV typu 2, powszechnie występującymi w Chinach. (Ryc. 5.)
Wiadomo, że stado było seropozytywne w zakresie przeciwciał PRVgE. Wcześniej zakażone lochy będą przez długi czas seropozytywne dla PRV gE i będą przekazywać anty-GE Ab swoim prosiętom, czyniąc je seropozytywnymi dla PRV do 15 tygodnia życia. Dlatego też badanie Ab u młodych prosiąt nie jest przydatne do diagnozowania choroby, gdy lochy są w większości seropozytywne. W przypadku braku zrozumienia faktu utrzymywania się matczynych przeciwciał gE, mogą być stawiane fałszywie dodatnie rozpoznania PRV.
Wyniki
W gospodarstwie stwierdzono, że do stada hodowlanego weszły loszki PRV dodatnie, a zagrożenie ASF zniechęciło do rutynowych szczepień przeciwko tej chorobie. Błąd w programie szczepień przeciwko PRV został napraiony i ferma nie odnotowała więcej podobnych przypadków.
![Ryc. 5. Drzewo filogenetyczne PhyML, PRV gE przedstawiające szczepy typu 1 (kaplan/becker -like), "klasyczne" szczepy typu 2 (Fa/SC/Ea-like) oraz szczepy o zwiększonej zjadliwości typu 2 (TJ/hb1201-like). Najnowsze PRV, ten przypadek [20-1048] i PRV ludzkiego zapalenia mózgu hSD1-2019 łączą się w grupy z TJ/hb1201.](https://www.3trzy3.pl/3tres3_common/art/pl/5016/drzewo-filogenetyczne-phyml-prv-ge_247317.png?w=820&q=1&t=1653979446)
Ryc. 5. Drzewo filogenetyczne PhyML, PRV gE przedstawiające szczepy typu 1 (kaplan/becker -like), "klasyczne" szczepy typu 2 (Fa/SC/Ea-like) oraz szczepy o zwiększonej zjadliwości typu 2 (TJ/hb1201-like). Najnowsze PRV, ten przypadek [20-1048] i PRV ludzkiego zapalenia mózgu hSD1-2019 łączą się w grupy z TJ/hb1201.
Dyskusja
Wścieklizna rzekoma (PRV), zwana również "chorobą Aujeszky'ego" (AD), została opisana jako śmiertelna choroba neurologiczna bydła w 1813 roku i była często mylona ze wścieklizną u bydła i psów. Ze względu na intensywny, niepohamowany świąd wywołany uszkodzeniem nerwów, choroba ta była znana jako "szalony świąd", ale czasami nazywano ją również "zakaźnym porażenie opuszkowe". W latach trzydziestych XX wieku R. E. Shope stwierdził, że wścieklizna rzekoma w Europie i szalony świąd w USA to ta sama choroba, szeroko rozpowszechniona i endemiczna u świń w większości krajów produkujących trzodę chlewną.
Świnia jest naturalnym gospodarzem wirusa PRV. Zakażenie może być łagodne i prawie niewidoczne lub może powodować wybuch epidemii z wysoką śmiertelnością. Różnice w obserwowanej zjadliwości wirusa PRV wynikają ze zmienności szczepu wirusa, czynników zwierzęcych oraz czynników losowych.
Objawy PRV u świń hodowlanych to choroba układu oddechowego i wirusowy zespół rozrodczy z poronieniami, obumieraniem zarodków, niepowodzeniami w przebiegu porodów, mumifikacje, słabymi noworodkami i niepłodnością loch.
Nie opisywano wcześniej przypadków objawów ocznych zakażenia wirusem PRV u świń.
U prosiąt w wieku poniżej 6 tygodni mogą wystąpić objawy neurologiczne, drżenie, ataksja, drgawki, biegunka, zaburzenia oddychania i wysoka śmiertelność. Prosięta zarażone w okresie ssania często mają białe ogniska martwicy na migdałkach, wątrobie, a czasami śledzionie. U starszych świń zazwyczaj występują objawy ze strony układu oddechowego: kaszel, duszność i uogólniony zespół oddechowy świń, jeśli jest on powikłany współistniejącymi problemami, takimi jak zakażenie mykoplazmozą, App, Strep, CSF, wrzody żołądka i wadliwą wentylacją. Objawy ze strony OUN (ośrodkowego układu nerwowego) występują sporadycznie u rosnących świń z PRV, ale raczej rzadko u zwierząt w wieku hodowlanym. Na nerkach mogą być widoczne wybroczyny. PCV2, klasyczny pomór świń (CSF), afrykański pomór świń (ASF) i PRRS mogą być uwzględnione w rozpoznaniu różnicowym lub mogą być zakażeniami współistniejącymi.
PRV rozprzestrzenia się pionowo przez stale zakażone lochy, przez sprzęt, brudne ciężarówki i urządzenia oraz przez zakażone zwierzęta hodowlane. Zakażone świnie rosnące łatwo rozprzestrzeniają PRV drogą oddechową. W chłodnym, wilgotnym powietrzu może dochodzić do przenoszenia aerozoli na odległość kilku kilometrów.
PRV można zaobserwować u zwierząt innych niż świnie, szczególnie u bydła, owiec, norek, psów i kotów. Podatne na zakażenie są wylęgające się kurczęta. Na fermach świń zakażonych wirusem PRV zaobserwowano odporne psy; ogólnie psy są podatne na zakażenie, które kończy się śmiercią po wystąpieniu objawów ze strony OUN.
Czy chorobę Aujeszkyego należy uznać za zoonozę?
Ludzie są stosunkowo odporni. Zakażenie u ludzi jest niezwykle rzadkie, chociaż wirus replikuje się w hodowanych komórkach ludzkich. Zgłaszane są przypadki zakażenia ludzi w wyniku kontaktu z kotami i psami, z łagodnymi objawami klinicznymi, z wyzdrowieniem i serokonwersją. Ostatnio w Chinach wśród opiekunów świń, lekarzy weterynarii i pracowników rzeźni udokumentowano kilka poważnych przypadków zapalenia mózgu i zapalenia wewnątrznaczyniowego. Z takimi poważnymi zakażeniami u ludzi wiąże się zwykle jakaś historia urazu lub kontuzji. Wirus wykryty w ostatnich przypadkach PRV u ludzi jest bardzo podobny do PRV wykrytego w tym przypadku (Rysunek 5).
Czy dostępne są dobre i skuteczne szczepionki?
Szczepienia są skuteczne w ograniczaniu nasilenia i rozprzestrzeniania się PRV. PRV jest możliwy do zwalczenia przy zastosowaniu obecnej technologii, ale występuje endemicznie w większości głównych prowincji Chin, w których hoduje się świnie, z częstością występowania w poszczególnych stadach dochodzącą do 60% na obszarach o wysokim zagęszczeniu świń. W chińskich gospodarstwach dostępne są szczepionki zabite (KV) i zmodyfikowane szczepionki żywe (MLV), a większość stad szczepi się przeciwko chorobie Aujeszkyego. Większość szczepionek PRV stosowanych na świecie zawiera delecję w genie gE, co w przypadku szczepionek atenuowanych czyni szczepionkę awirulentną i umożliwia rozróżnianie zwierząt zakażonych i szczepionych (DIVA). Pierwszymi szczepionkami z delecją gE były awirulentna żywa szczepionka przeciw nosówce (K) Bartha (1961) oraz szczepionka bukareszteńska (Buk) znana pod nazwą "Norden". Obecnie stosuje się szczepionki PRV z całkowitą lub częściową delecją gE. W przypadku stosowania strategii DIVA oraz warunków sanitarnych/izolacji przy produkcji seryjnej typu "wszystko w jednym" szczepionka jest przydatnym narzędziem do eliminacji i zwalczania choroby. Szczepionka nie wywołuje odporności sterylizującej ani nie tworzy wokół świni "magicznej bańki" chroniącej ją przed zakażeniem w warunkach terenowych. Jednakże, lochy wielokrotnie szczepione przeciwko PRV wytwarzają bierną odporność humoralną, która chroni świnie przed zakażeniem aż do okresu poodsadzeniowego. Jest mało prawdopodobne, aby wielokrotnie szczepione lochy przekazywały wirusa PRV swoim prosiętom lub wprowadzanym do stada naiwnym lub prawie naiwnym loszkom. Szczepionki zawierające zabitego wirusa (KV) są bardziej skuteczne niż atenuowane szczepionki przypominające, ale doświadczenie pokazuje, że atenuowana szczepionka może być "wystarczająco dobra" jako szczepionka przypominająca w sytuacjach, gdy szczepionka KV jest niedostępna. W przypadku, gdy loszki pochodzące od szczepionych loch są szczepione i hodowane w partiach typu "całe puste- całe pełne" (all-in/all-out) i wchodzą do stada szczepionych loch, mogą one pozostać ujemne i zastąpić starsze zakażone lochy w drodze eliminacji. Dzięki tej metodzie PRV został wyeliminowany w licznych stadach, na wielu obszarach i w całych krajach.
Bardziej zjadliwa wścieklizna rzekoma
Od około 2011 roku w Chinach odnotowuje się występowanie wariantów o zwiększonej zjadliwości (EV) wirusa rzekomej wścieklizny. "Zachodnie" szczepy PRV, takie jak Kaplan, Becker i Bartha, należą do grupy typu 1. (Ryc. 5) Należy zauważyć, że szczep Bartha K-61 ma całkowicie usuniętą część gE. "Klasyczne" PRV Chin/Azji {Ea, Fa, SC} należą do typu 2. Warianty szczepów typu 2 {TJ, hb1201, jsy7-2021, ...} są zaangażowane w ostatnie ogniska wścieklizny rzekomej o "zwiększonej zjadliwości" (o cięższym przebiegu niż klasyczny typ 2). PRV z ludzkiego zapalenia mózgu/ftalmitis, takie jak ten: GenBank: MT469550 (hSD1-2019) łączą się z wirusem 20-1048 wykrytym w tym niezwykłym przypadku, jak również ze szczepami EV. (Ryc. 5). Część zwiększonej zjadliwości może być spowodowana zmianami w glikoproteinie gE, dla której szczepionki delecyjne typu Bartha nie stymulują odporności, lub zmianami w innych loci.
Wyeliminowanie PRV jest możliwe i wykonalne, ma istotne implikacje dla zrównoważonego rozwoju, bezpieczeństwa żywnościowego i zdrowia ludzi, a także wyeliminowałoby ważne źródło strat dla gospodarstw utrzymujących świnie.














