Wstęp
Farma komercyjna z pogłowiem 600 loch mieściła się w Irlandii, a w ciągu roku powiększyła się do 1000 loch.
Protokół szczepień jest przedstawiony w Tabeli 1.

Tabela 1. Program szczepień
| Szczepienie | Loszki | Lochy | Knury | Prosięta |
| Parwowirus | iniekcja 2 ml @ selekcja | iniekcja 2 ml 2 tyg. po porodzie | iniekcja 2 ml dwa razy w roku | |
| Różyca | iniekcja 2 ml @ selekcja i 2 tyg. przed kryciem | iniekcja 2 ml 2 tyg. po porodzie | iniekcja 2 ml dwa razy w roku | |
| Kolibacilloza i klostridioza | iniekcja 2 ml 6 i 2 tyg. przed porodem | iniekcja 2 ml 2 tyg. przed porodem | ||
| PRRS (MLV) | iniekcja 2 ml @ selekcja i @ 60 dni po kryciu | iniekcja 2 ml w 6 dni po porodzie i @ 60 dni po kryciu | iniekcja 2 ml dwa razy w roku | |
| PCV-2 | iniekcje 1 ml przy odsadzeniu | |||
| Enzoot. zap. płuc | 1 ml @ 10 - 14 dniu ż. i @ odsadzenia |
Loszki pochodzą z własnego chowu. Knury służą do stymulacji. Loszki i lochy są poddawane sztucznej inseminacji z jednego źródła.
Najbliższa ferma świń oddalona jest od obiektu o 2 km.
Historia
Rolnik skontaktował się z lekarzem weterynarii w sprawie zwiększenia niewydolności oddechowej i utraty kondycji ciała wraz ze wzrostem śmiertelności u prosiąt odsadzonych i rosnących.
Podjęte kroki
Badanie kliniczne
Podczas wizyty w gospodarstwie we wrześniu 2017 r. przebywało wiele świń w wieku od 6 do 15 tygodni z klinicznymi objawami utraty kondycji i oddychaniem brzusznym (ryc. 1 i 2). Kaszel był bardzo słabo wyrażony. Kojce były przepełnione.

Ryc 1. Stłoczone świnie po odsadzeniu, wśród których są zwierzęta z objawami choroby

Ryc 2. Zwierzęta w złej kondycji
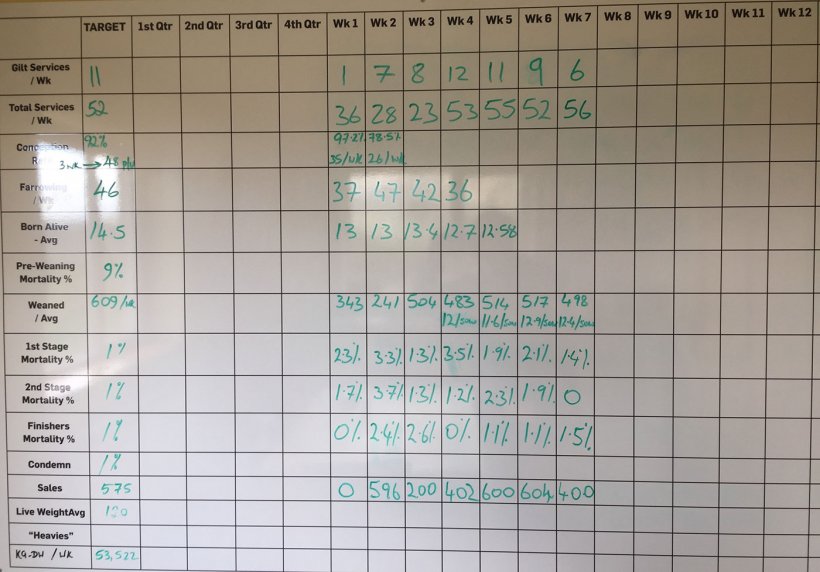
Według hodowcy śmiertelność od odsadzenia do końca tuczu wynosiła od 3,5 do 5%. Jednak podana wartość była zupełnie inna niż ta na cotygodniowej tablicy ściennej na stołówce (ryc. 3).
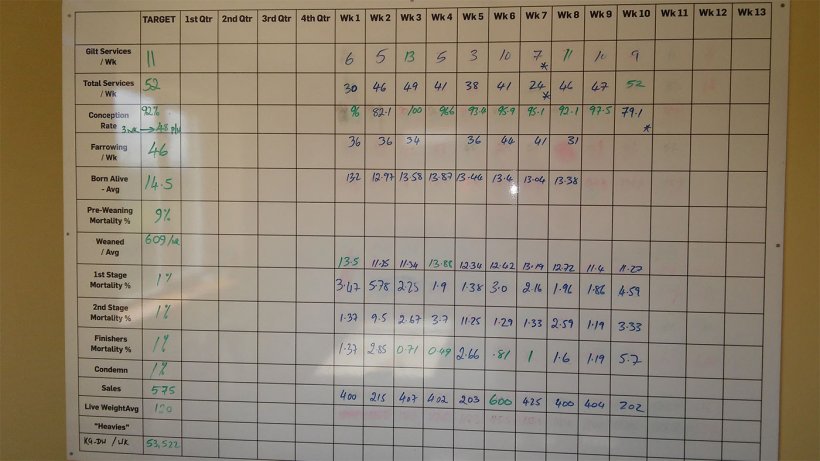
Ryc 3. Wyniki tygodniowe, aż do września 2017.
Śmiertelność od odsadzenia do końca tuczu wyniosła 8,48% w ciągu ostatnich 10 tygodni przy analizie danych z tablicy. Ta śmiertelność została ujawniona jako 2.64% w 1. etapie (od 4 do 9 tygodni); 3,82% w drugim etapie (od 10 do 15 tygodni); oraz 1,83% pod koniec tuczu (od 16 tygodnia życia do uboju).
Badanie laboratoryjne
Dwie 6-tygodniowe świnie oddychające brzusznie,z utratą kondycji ciała zostały poddane eutanazji w celu badania pośmiertnego w gospodarstwie (ryc. 4 i wideo 1). Próbki zostały zebrane i przesłane do laboratorium w celu przeprowadzenia dalszych analiz.

Ryc 4. Prosię odsadzone z objawami oddechowymi i złą kondycją
Wideo 1. Prosię po odsadzeniu z dusznością i utratą kondycji.
Wyniki badań pośmiertnych i laboratoryjnych zestawiono w Tabeli 2. Fotograficzne dane pośmiertne przedstawiono na ryc. 5, 6, 7 i 8.
Tabela 2. Wyniki laboratoryjne dwóch 6-tygodniwych świń.
| Prosię | Sekcja | Bacteriologia | Badania molekularne | Histologia |
| 1 | Zła kondycja ciała. Niedowaga. Pericarditis. Zap. opłucnej. Stwardnienie w obrębie płatów brzusznego, sercowego i przeponowego z śródmiąższowym zapaleniem płuc. |
Pasteurella multocida. (Płuca). Streptococcus suis serotyp 3. (Płuca). |
Ujemne na Mycoplasma hyopneumoniae, Influenza Virus typ A & PCV-2 w RT-PCR (Płuca). EU-PRRS dodatnie w RT-PCR (CT: 21.2) dla puli płuc od prosiąt 1 i 2. |
Oskrzela z naciekiem nautrofili i hiperplazją nabłonka oskrzeli. Tkanka płuc wykazuje różne stadia włóknikowego, odoskrzelowego zapalenia płuc. Widoczne w wielu miejscach zwątrobienie i stwardnienie mięsiste. Proliferacja tkanki włóknistej jest wieloogniskowa, obecna w przestrzeniach międzypęcherzykowych i międzypłatowych. Zmiany są reprezentatywne dla przewlekłego stanu zapalnego. |
| 2 | Zła kondycja ciała. Niedowaga. Powiększenie w. chł. pachwinowych. Pericarditis, zap. opłucnej. Stwardnienie w obrębie płatów brzusznego, sercowego i przeponowego z śródmiąższowym zapaleniem płuc. |
Pasteurella multocida. (Płuca). | Ujemne dla Mycoplasma hyopneumoniae, Influenza Virus typ A & PCV-2 w RT-PCR (Płuca). EU-PRRS dodatnie w RT-PCR (CT: 21.2) dla puli płuc od prosiąt 1 i 2. |
Oznaki przewlekłego zapalenia płuc. Zapalenie jest typu nieżytowo- ropnego. Oskrzela są wypełnione neutrofilami, a nabłonek oskrzeli z cechami hiperplazji. Na przewlekły stan wskazuje proliferacją tkanki włóknistej w przestrzeni śródmiąższowej. Opłucna z ogniskową hiperplazją, można znaleźć obrzęk śródmiąższowy. |
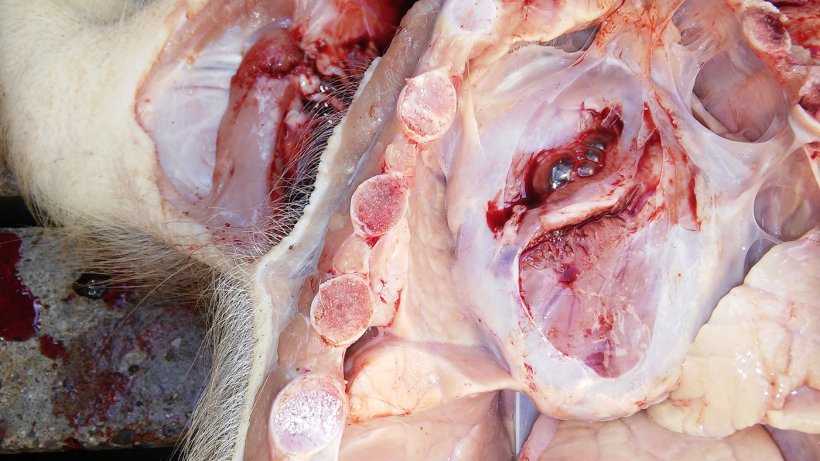
Ryc 5. Pericarditis (zapalenie osierdzia).
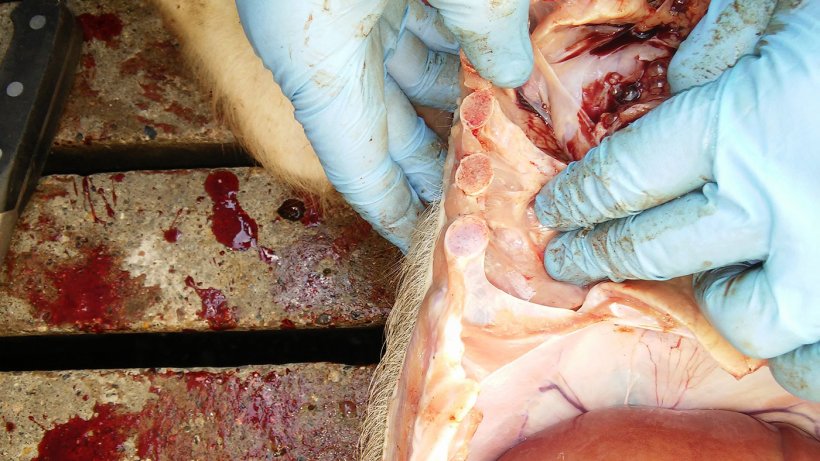
Ryc 6. Zapalenie opłucnej między opłucną płucną a opłucną klatki piersiowej.

Ryc 7. Śródmiąższowe zapalenie płuc ze stwardnieniem płata przeponowego
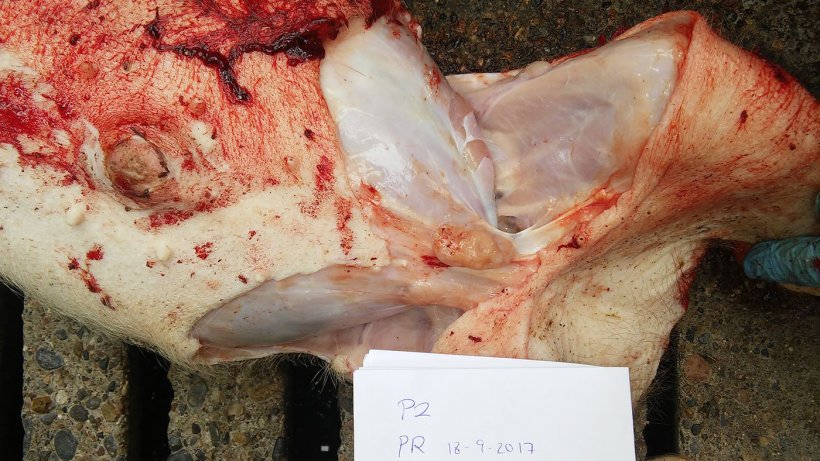
Ryc 8. Powiększony węzeł chłonny krezkowy.
Diagnostyka różnicowa
W oparciu o badanie kliniczne i laboratoryjne przygotowano poniższą listę diagnostyki różnicowej:
- PRRS (Porcine Reproductive and Respiratory Syndrome- zespół rozrodczo- oddechowy świń).
- PCV2 (Porcine Circovirus type 2- cirkowirus świń typu 2 ).
- Influenza Virus typ A. ( Typ A wirusa grypy)
- Enzootyczne zapalenie płuc (Mycoplasma hyopneumoniae)
Czynniki wirusowe, takie jak wirus grypy typu A i PCV-2, zostały wykluczone na podstawie negatywnych wyników laboratoryjnych. Protokół szczepień przeciwko PCV-2 był zadowalający w tej jednostce.
Enzootyczne zapalenie płuc zostało wykluczone w wyniku negatywnych wyników laboratoryjnych, satysfakcjonującego programu szczepień i braku kaszlu w stadzie.
Na podstawie historii oraz spójnych badań klinicznych i laboratoryjnych wskazano rozpoznanie zakażenia PRRS i wtórną oportunistyczną infekcję bakteryjną w stadzie.
Program kontroli
Zasugerowano szczepienie szczepionką MLV-PRRS wszystkich prosiąt w wieku 10-14 dni.
Wynik programu kontroli
Obawy ze strony układu oddechowego i zła kondycja świń zostały zmniejszone. Śmiertelność spadła znacząco do 5,2% w trzy miesiące później. Ta śmiertelność wynosiła 2,25% w 1. etapie (od 4 do 9 tygodni); 1,72% w drugim etapie (od 10 do 15 tygodni); oraz 1,24% pod koniec tuczu (od 16 tygodnia życia do uboju) (rys. 10). Gęstości obsady nigdy nie została zmieniona.
Ryc 10. Wyniki tygodniowe, aż do lutego 2018.
Dyskusja
Pod koniec lat 80. XX w. opisano ostre zaburzenia rozrodczości i układu oddechowego u świń w Stanach Zjednoczonych (Keffaber 1989). W tym czasie czynnik etiologiczny był nieznany. Ten sam zespół objawów został opisany w Niemczech w 1990 r. (OIE 1992). Czynnik etiologiczny został po raz pierwszy wyizolowany w Holandii w 1991 r. (Wensvoort i in. 1991) i nazwany zespołem rozrodczo- oddechowym świń (PRRS) (Terpstra i in. 1991).
Zakażenie PRRS w Irlandii Północnej zostało po raz pierwszy zdiagnozowane w 1997 roku (Anonim 1997) oraz w Republice Irlandii w 1999 roku (Ohlinger i inni 2000).
PRRS jest obecny w większości krajów produkujących świnie na świecie z kilkoma wyjątkami. Kraje takie jak Szwecja (Carlsson i inne 2009), Norwegia (OIE 1997), Finlandia (Bøtner 2003), Szwajcaria (Corbellini i inne 2006), Nowa Kaledonia (OIE 1996), Nowa Zelandia (Motha i inne 1997), Australia (Garner i inne 1997), Argentyna (Perfumo i Sanguinetti 2003), Brazylia (Ciacci-Zanella i inni 2004) i Kuba (Alfonso i Frias Lepoureau 2003) są wolne od PRRS.
Nasilenie infekcji PRRS różni się w zależności od fermy. Czynniki niezakaźne zaostrzają ekspresję objawów klinicznych. Te czynniki niezakaźne obejmują zarządzanie, przepływ trzody chlewnej, regulację temperatury i system utrzymania (Zimmerman i in. 2012). Jednoczesne zakażenia niektórymi czynnikami wirusowymi i bakteryjnymi wyzwalają lub zwiększają nasilenie objawów klinicznych PRRS (Shibata i inni 2003, Thacker i inni 1999, Borobia i inni 2014). Zapalenie opłucnej jest jednym z uszkodzeń wywołanych przez wirusa PRRS (Muirhead i Alexander 1997). BPEX (2009) stwierdził, że znaczenie ekonomiczne takich zmian jest znaczące. Zwiększona częstość występowania zapalenia opłucnej wiązała się ze zmniejszoną wagą tuszy i zwiększonym wiekiem przy uboju. Koszt dla producenta, dla typowej 10% częstości występowania zapalenia opłucnej na poziomie partii, wynosi 2,26 £ na świnie, na podstawie zmniejszonej masy tuszy i zwiększonego wieku przy uboju.
Szczepionka MLV PRRS okazuje się przydatna w ograniczaniu skutków wirusa terenowego u świń odsadzonych (Waddell i in. 2008), jak w tym przypadku klinicznym.






