Choroba Glassera nadal występuje na fermach trzody chlewnej, a istotność dokładnej diagnozy ostatnio bardzo wzrosła ze względu na naciski na zmniejszenie zużycia antybiotyków. Choroba jest wywoływana przez bakterię Haemophilus parasuis, która wywołuje systemową infekcję u swojego jedynego gospodarza, świni, co skutkuje włóknikowym zapaleniem błon surowiczych. Jednak H. parasuis nie jest jedyną bakterią, która może powodować wymienione zmiany u świń, co tym bardziej podkreśla istotność diangostyki różnicowej, która pozwoli na określenie czynnika sprawczego zmian i choroby. Identyfikacja czynnika sprawczego pozwala na wdrożenie środków zapobiegawczych bez użycia antybiotyków- jak na przykład wdrożenie programu szczepień- lub jeśli zachodzi taka potrzeba zastosowanie antybiotyków skutecznych przeciwko wyizolowanemu szczepowi. Prewalencja choroby Glassera jest wysoka na odchowalni ze względu na wysoki poziom stresu spowodowany odsadzeniem od matki i adaptacją do nowej paszy, transportem i mieszaniem z innymi zwierzętami.
Typowe zmiany zapalne błon surowiczych u prosiąt na odchowalni mogą być wywołane przez różne bakterie. Izolacja bakterii ze zmienionych miejsc jest najlepszym sposobem na poznanie czynnika sprawczego, dodatkowo pozwala na dokładniejszą charakterystykę szczepu, jak na przykład określenie wirulencji metodą PCR (Olvera et al., 2012) lub zbadanie wrażliwości na leki. Diagnostyka różnicowa obejmuje głównie Streptococcus suis, ale coraz częściej także Mycoplasma hyorhinis (Fot 1). Nieprawidłowe rozpoznanie H. parasuis jako czynnika sprawczego, w oparciu tylko o obraz kliniczny, może prowadzić do wprowadzenie nieskutecznej antybiotykoterapii. Efektem stosowania nieskutecznych leków może być wywołanie u zwierząt dysbiozy, co sprawi, że będą wrażliwsze na kolejne zakażenia. Zastosowanie niewłaściwych antybiotyków nie tylko nie przyniesie spodziewanego efektu terapeutycznego, ale także może przyczynić się do późniejszego pogorszenia zdrowotności zwierząt.

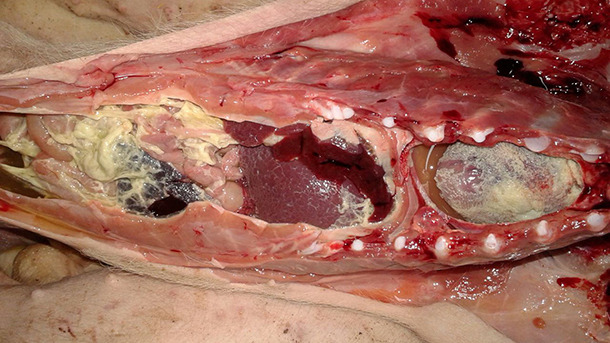
Fot 1.Włóknikowe zapalenie błon surowiczych u prosięcia. Nie wykryto Haemophilus parasuis. Z płynu w jamie brzusznej i osierdzia wyizolowano Mycoplasma hyorhinis .
Wdrożenie immunizacji może również wymagać wykonania pełnej diagnozy wstępnej, z prawidłową identyfikacją i charakterystyką czynnika sprawczego. Jeśli diagnoza choroby Glassera została postawiona jedynie na podstawie zaobserwowania zapalenia błon surowiczych, a zmiany te faktycznie są wywołane przez M. hyorhinis lub S. suis, oczywiste jest, że szczepienie przeciwko H. parasuis nie pomoże w eradykacji choroby ze stada. Identyfikacja patogenu w laboratorium powinna być obowiązkowym krokiem w doborze najwłaściwszej terapii i kontroli choroby. Ponadto biorąc pod uwagę zmienność H. parasuis, charakterystyka szczepu może mieć duże znaczenie. Ostatnio rozwinięta metoda serotypowania za pomocą PCR jest krokiem naprzód pozwalającym na określenie serotypu izolowanych szczepów H. parasuis (Fot. 2; Howell et al., 2015). Ta technika rozwiązuje wcześniejszy problem, kiedy to niewiele laboratoriów było w stanie serotypizowwać H. parasuis klasycznymi metodami serologicznymi. Co więcej, technika ta jest podstawą do wdrożenia immunizacji, ponieważ obecne na rynku szczepionki zapewniają ochronę tylko przed wybranymi serotypami.
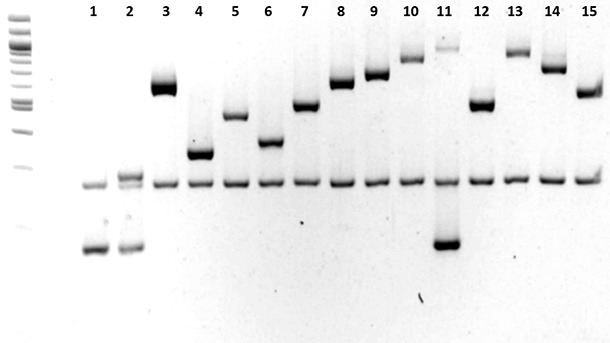
Fot 2. Serotypowanie Haemophilus parasuis (1 do 15) metodą PCR. Howell et al., 2015.
Patogeny, które często wywołują zapalenie błon surowiczych u prosiąt na odchowalni stosunkowo wcześnie kolonizują górne drogi oddechowe prosiąt. Źródłem infekcji pozostają lochy, a ich status immunologiczny i zakaźny odpowiada za utrzymywanie się zakażenia na fermie. W przypadku H. parasuis oczywistym jest, że nie ma zjadliwych szczepów, które mogą być izolowane od zdrowych prosiąt. Kolonizacja przez te szczepy może chronić je przed kolejnymi infekcjami zjadliwymi szczepami (Brockmeier et al., 2013). Dane te potwierdzają słuszność wykorzystania sztucznej kolonizacji prosiąt przez dobrze poznany, niewirulentny szczep w celu zwalczania choroby Glassera. Jest to strategia, która zasługuje na dalsze badania, co byłoby naturalną alternatywą dla antybiotyków
Wyniki klinicznej infekcji H. parasuis będą w dużym stopniu zależały od zjadliwości szczepów bakterii, lecz także od obecności innych patogenów w stadzie. Dlatego pojawienie się zapalenia błon surowiczych związanego z infekcjami wirusem grypy lub PRRS nikogo nie dziwi. W tym ostatnim przypadku zaleca się, aby kontrolować główny czynnik, wirusowy, ponieważ taka infekcja wywołuje immunosupresję, ułatwiając wtórnego zakażenia bakteryjne, w tym wypadku H. parasuis.
Podsumowując, przeprowadzenie kompletnej i dokładnej diagnozy jest niezbędne do zwalczania choroby Glassera, co obecnie jest ułatwione przez nowe rozwiązania technologiczne, które pozwalają na łatwe określenie zjadliwości i serotypu szczepów H. parasuis.




